Apparecchiature e sistemi per camere bianche biofarmaceutiche ad alte prestazioni
QUALIA fornisce attrezzature avanzate per camere bianche biofarmaceutiche, progettate per soddisfare i più severi requisiti di sicurezza e normativi del settore. La nostra gamma completa di soluzioni comprende sistemi di contenimento specializzati per laboratori BSL-3 e BSL-4, che integrano tecnologie all'avanguardia con design pratici che migliorano sia la sicurezza che l'efficienza operativa. Grazie alla nostra esperienza decennale nell'infrastruttura delle camere bianche e nelle misure di protezione OEB, forniamo alle aziende farmaceutiche e biotecnologiche attrezzature affidabili che assicurano una protezione completa durante i processi produttivi critici.
Progettazione collaborativa e
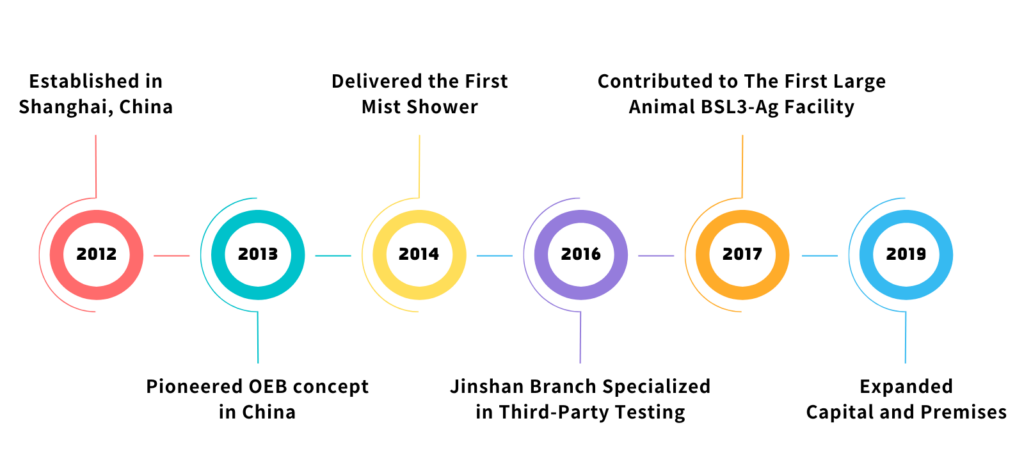
Costruzione della prima sala per grandi animali BSL3-Ag della Cina.
Ha fornito servizi di base ad oltre 70 laboratori BSL3 globali e a laboratori di produzione di vaccini.
Una rete globale di oltre 210 clienti, potenziata da partnership strategiche di collaborazione.
Ha fornito oltre 1800 porte APR, 930 docce a nebbia, 850 BIBO e 400 passbox VHP.
Requisiti di convalida delle camere bianche biofarmaceutiche
L'implementazione di adeguati requisiti di convalida delle camere bianche biofarmaceutiche è essenziale per mantenere la conformità normativa e l'integrità del prodotto. I nostri protocolli di convalida assicurano che le apparecchiature della camera bianca soddisfino i rigorosi standard del settore e favoriscano l'efficienza operativa.
R&S avanzata
Prodotti all'avanguardia sviluppati da un team globale di esperti.
Marchio affidabile
Relazioni di lunga data con una base di clienti fedeli nei settori farmaceutico e sanitario.
Competenza nella protezione
Ampia esperienza con gli standard di laboratorio P3, P4 e le normative industriali OEB.
Soluzione unica
Progetti completi chiavi in mano per camere bianche e attrezzature associate.
Capacità di QUALIA
Attrezzature e soluzioni per camere bianche
Serie Aria
Sistema di filtrazione in situ
Serie ISO
cRABS
Isolatore OEB4/5
Isolatore di biosicurezza
Serie di serrature
Serranda di isolamento di biosicurezza
Porte APR a tenuta meccanica
Guarnizione pneumatica per porte APR
Modulo Laboratorio
Laboratorio modulo mobile
Serie Pass
Vasca di biosicurezza
VHP Pass Box
Cassetta di sicurezza biologica
Serie doccia
Doccia a nebbia
Doccia chimica
Doccia d'acqua
Serie di serrature
Generatore VHP tipo I
Generatore VHP Tipo II III
Trattamento dell'acqua
Condotto in situ HEPA
Bag-In/Bag-Out - Sistemi BIBO in ambienti BSL-3/BSL-4

Una tipica sostituzione del filtro BIBO prevede la sigillatura del sacchetto esterno all'alloggiamento, la rimozione del filtro usato nel sacchetto interno, quindi la sigillatura e la rimozione del filtro in sacchetto per uno smaltimento sicuro. Questo processo è supportato da porte per guanti e da chiare SOP, che riducono al minimo l'errore umano e il rischio di esposizione. Il risultato è una procedura convalidata e ripetibile che soddisfa o supera gli standard internazionali di biosicurezza e ingegneria come ISO 14644, ASME AG-1 e IEST-RP-CC001.
Soluzioni di contenimento complete per la produzione biofarmaceutica
La produzione biofarmaceutica richiede un controllo senza compromessi del particolato aereo, della contaminazione incrociata e dell'esposizione professionale. Le soluzioni di contenimento complete integrano più livelli di controlli tecnici, tra cui sistemi BIBO, filtrazione dell'aria particolata ad alta efficienza (HEPA/ULPA), zone a pressione negativa e isolatori personalizzati. Questi sistemi sono progettati per proteggere l'integrità del prodotto e la sicurezza del personale lungo l'intera catena del processo, dalla movimentazione delle materie prime al confezionamento del prodotto finale.
Queste soluzioni sono progettate per essere conformi agli standard globali, come l'Allegato 1 delle GMP dell'UE, la FDA 21 CFR Parte 211 e la ISO 14644. Il risultato è un ambiente di produzione che supporta le ispezioni normative, riduce il rischio di perdita di lotti e migliora la produttività complessiva.
IOS 14644
Standard della camera bianca
Unità di filtrazione BIBO per tutti i flussi critici di aria di scarico e di alimentazione, garantendo una manutenzione sicura dei filtri e un contenimento convalidato.
Isolatori e sistemi di barriera personalizzati per la lavorazione asettica, la manipolazione degli API e la gestione dei composti potenti.
Gestione della cascata di pressione per mantenere un flusso d'aria direzionale e prevenire la contaminazione incrociata tra zone pulite e sporche.
Monitoraggio ambientale continuo per il rilevamento in tempo reale del numero di particelle, delle deviazioni di pressione e delle prestazioni del sistema.
Protocolli di decontaminazione convalidati per le superfici delle apparecchiature e delle strutture, favorendo un cambio rapido e riducendo al minimo i tempi di inattività.
Misure di protezione e standard di sicurezza OEB
Le misure di protezione OEB (Occupational Exposure Band) sono essenziali per salvaguardare il personale che lavora con ingredienti farmaceutici attivi ad alta potenza (HPAPI) e composti pericolosi. Le moderne soluzioni di contenimento sono progettate per soddisfare i severi requisiti OEB, fornendo una protezione stratificata attraverso controlli ingegneristici, processi convalidati e monitoraggio continuo.
Gli elementi chiave delle misure di protezione dell'OEB includono:
Dispositivi di trasferimento a sistema chiuso e isolatori a guanto per eliminare il contatto diretto dell'operatore con i materiali pericolosi.
Sistemi BIBO per la manutenzione dei filtri, assicurando che tutti i materiali contaminati siano contenuti in modo sicuro e smaltiti senza rischi di esposizione.
Ambienti a pressione negativa e i sistemi di ingresso delle camere di compensazione per prevenire la diffusione di contaminanti aerodispersi.
Protocolli di pulizia e decontaminazione convalidati per tutte le attrezzature e le superfici a contatto con i composti potenti.
Monitoraggio dell'ambiente e dell'esposizione in tempo reale per garantire che le concentrazioni nell'aria rimangano entro le soglie accettabili dell'OEB.
La conformità agli standard di sicurezza OEB è confermata da rigorose valutazioni del rischio, dalla qualificazione delle prestazioni e dalla convalida continua. Standard internazionali come ISPE Good Practice Guide, ICH Q9 Quality Risk Management e ISO 45001 Occupational Health and Safety Management Systems forniscono il quadro di riferimento per la progettazione e il mantenimento di strategie di contenimento conformi.
Bilancio di esercizio
Esplorate la nostra Galleria dei trionfi: Immergetevi nella nostra selezione di progetti di successo recenti, in cui il nostro approccio mirato e la nostra esperienza hanno portato a risultati positivi per i nostri clienti. Ogni caso testimonia il nostro impegno nel fornire soluzioni solide ed efficaci.

Informazioni su QUALIA
QUALIA è composta da un gruppo di 42 esperti nel campo dell'ingegneria farmaceutica e della biosicurezza. La nostra profonda esperienza comprende la progettazione, la costruzione, la gestione e i servizi di consulenza e convalida sia locali che globali. Siamo fermamente intenzionati a fornire soluzioni complete su misura per l'ingegneria dei sistemi puliti di biosicurezza. Il nostro portafoglio comprende un assortimento di prodotti diversi, come dispositivi di purificazione, dispositivi di biosicurezza, sistemi HVAC, sistemi di automazione, servizi di convalida, apparecchiature di processo e tubazioni sterili. Siamo orgogliosi della nostra capacità di ideare prodotti e sistemi proprietari che soddisfano in modo specifico le esigenze dei nostri clienti nei settori farmaceutico e della biosicurezza.
Domande frequenti
Come selezionare la giusta attrezzatura per camera bianca per la produzione farmaceutica?
Quando si scelgono le attrezzature per camere bianche per la produzione farmaceutica, si devono considerare tre fattori critici: la classificazione di pulizia richiesta (ISO 5-8), le esigenze di contenimento specifiche del processo e i requisiti di conformità alle normative. Valutare le apparecchiature in base alla compatibilità dei materiali con gli agenti detergenti, all'accessibilità della manutenzione e alla documentazione di convalida. I nostri specialisti del settore biofarmaceutico consigliano di condurre una valutazione completa dei rischi per identificare le potenziali fonti di contaminazione prima di finalizzare le specifiche delle apparecchiature.
Quali sono le principali differenze tra i sistemi BIBO e i filtri tradizionali?
I sistemi BIBO (Bag In Bag Out) offrono un contenimento superiore durante la sostituzione dei filtri rispetto agli alloggiamenti tradizionali, utilizzando un sistema di sacchi sigillati che impedisce il contatto diretto con i filtri contaminati. Questo riduce significativamente l'esposizione dell'operatore a materiali pericolosi e mantiene l'integrità della camera bianca durante la manutenzione. Gli alloggiamenti dei filtri tradizionali richiedono l'arresto dell'ambiente durante le sostituzioni, mentre i sistemi BIBO consentono un funzionamento continuo, migliorando l'efficienza e riducendo i tempi di inattività della produzione.
Con quale frequenza devono essere riconvalidate le apparecchiature per camere bianche?
Le apparecchiature per camere bianche biofarmaceutiche devono essere sottoposte a riconvalida secondo un programma basato sui rischi, in genere ogni anno per i sistemi critici e dopo qualsiasi modifica significativa. I sistemi di monitoraggio continuo possono fornire informazioni basate sui dati per ottimizzare la frequenza di riconvalida in base alle prestazioni effettive piuttosto che a scadenze arbitrarie. I requisiti normativi possono specificare intervalli minimi di riconvalida in base ai processi specifici e ai profili di rischio dei prodotti.
Quale livello di contenimento è appropriato per i composti OEB 4?
I composti OEB 4 richiedono soluzioni di contenimento complete, tra cui sistemi chiusi, ambienti a pressione negativa e tecnologie di barriera ridondanti. Il contenimento appropriato comprende sistemi di filtrazione BIBO dedicati, camere d'aria con meccanismi di interblocco delle porte e monitoraggio continuo delle pressioni differenziali. Il personale che lavora con i materiali OEB 4 deve utilizzare DPI adeguati e seguire rigorose procedure operative standard per la manipolazione dei materiali e i protocolli di decontaminazione.
In che modo i requisiti dei laboratori BSL-3 e BSL-4 differiscono per le attrezzature di contenimento?
I laboratori BSL-4 richiedono misure di contenimento molto più severe rispetto a BSL-3, tra cui armadi di sicurezza biologica di Classe III o tute a pressione positiva con forniture d'aria dedicate. Entrambi richiedono la filtrazione HEPA per l'aria di scarico, ma il BSL-4 richiede sistemi di filtrazione ridondanti con requisiti di convalida aggiuntivi. Le strutture BSL-4 devono implementare capacità di decontaminazione complete, mentre le BSL-3 possono utilizzare procedure di decontaminazione localizzate in base alla valutazione del rischio.