Équipements et systèmes de salles blanches biopharmaceutiques de haute performance
QUALIA fournit des équipements de salle blanche biopharmaceutique de pointe conçus pour répondre aux exigences les plus strictes en matière de sécurité et de réglementation dans l'industrie. Notre gamme complète de solutions comprend des systèmes de confinement spécialisés pour les laboratoires BSL-3 et BSL-4, intégrant une technologie de pointe avec des conceptions pratiques qui améliorent à la fois la sécurité et l'efficacité opérationnelle. Forts de plusieurs décennies d'expertise en matière d'infrastructures de salles blanches et de mesures de protection OEB, nous fournissons aux entreprises pharmaceutiques et biotechnologiques des équipements fiables qui garantissent une protection complète tout au long des processus de fabrication critiques.
Conception collaborative et
Construction de la première salle pour grands animaux BSL3-Ag en Chine.
Fourniture de services de base à plus de 70 laboratoires BSL3 et ateliers de production de vaccins dans le monde.
Un réseau mondial de plus de 210 clients, renforcé par des partenariats stratégiques de collaboration.
Il a fourni plus de 1800 portes APR, 930 douches à brouillard, 850 BIBO et 400 boîtes de passage VHP.
Exigences en matière de validation des salles blanches dans l'industrie biopharmaceutique
La mise en œuvre d'exigences appropriées en matière de validation des salles blanches biopharmaceutiques est essentielle pour maintenir la conformité réglementaire et l'intégrité des produits. Nos protocoles de validation garantissent que votre équipement de salle blanche répond aux normes rigoureuses de l'industrie tout en favorisant l'efficacité opérationnelle.
R&D avancée
Des produits de pointe développés par une équipe mondiale d'experts.
Marque de confiance
Des relations de longue date avec une clientèle fidèle dans les secteurs de la pharmacie et des soins de santé.
Expertise en matière de protection
Expérience approfondie des normes de laboratoire P3 et P4 et des réglementations industrielles de l'OEB.
Une solution unique
Projets clés en main complets pour les salles blanches et les équipements associés.
Capacité de QUALIA
Équipements et solutions pour salles blanches
Série Air
Système de filtration in situ
Série ISO
cRABS
OEB4/5 Isolateur
Isolateur de biosécurité
Série de serrures
Amortisseur d'isolement de biosécurité
Portes APR à garniture mécanique
Portes APR à joint pneumatique
Module Laboratoire
Laboratoire de modules mobiles
Série Pass
Réservoir de sécurité biologique
Boîte de passage VHP
Boîte de sécurité biologique
Série douche
Douche brumeuse
Douche chimique
Douche d'eau
Série de serrures
Générateur VHP Type I
Générateur VHP Type II III
Traitement de l'eau
Pipeline in situ HEPA
Bag-In/Bag-Out - Systèmes BIBO dans les environnements BSL-3/BSL-4

Un changement de filtre BIBO typique consiste à sceller le sac extérieur au boîtier, à retirer le filtre usagé dans le sac intérieur, puis à sceller solidement et à retirer le filtre ensaché pour le mettre au rebut en toute sécurité. Ce processus est soutenu par des ports de gants et des procédures opératoires normalisées claires, ce qui minimise l'erreur humaine et le risque d'exposition. Le résultat est une procédure validée et reproductible qui respecte ou dépasse les normes internationales de biosécurité et d'ingénierie telles que ISO 14644, ASME AG-1 et IEST-RP-CC001.
Solutions complètes de confinement pour la fabrication de produits biopharmaceutiques
La fabrication biopharmaceutique exige un contrôle sans compromis des particules en suspension dans l'air, de la contamination croisée et de l'exposition professionnelle. Les solutions de confinement complètes intègrent plusieurs couches de contrôles techniques, y compris les systèmes BIBO, la filtration des particules d'air à haute efficacité (HEPA/ULPA), les zones de pression négative et les isolateurs personnalisés. Ces systèmes sont conçus pour protéger l'intégrité des produits et la sécurité du personnel tout au long de la chaîne de traitement, de la manipulation des matières premières à l'emballage du produit final.
Ces solutions sont conçues pour être conformes aux normes internationales telles que l'annexe 1 des BPF de l'UE, la partie 211 du CFR de la FDA et la norme ISO 14644. Il en résulte un environnement de fabrication qui prend en charge les inspections réglementaires, réduit le risque de perte de lots et améliore la productivité globale.
IOS 14644
Norme de salle blanche
Unités de filtration BIBO pour tous les flux d'air d'extraction et d'alimentation critiques, ce qui garantit une maintenance sûre des filtres et un confinement validé.
Isolateurs et systèmes de barrières sur mesure pour le traitement aseptique, la manipulation des IPA et la gestion des composés puissants.
Gestion de la cascade de pression pour maintenir un flux d'air directionnel et éviter la contamination croisée entre les zones propres et les zones sales.
Surveillance continue de l'environnement pour la détection en temps réel du nombre de particules, des écarts de pression et des performances du système.
Protocoles de décontamination validés pour les surfaces des équipements et des installations, ce qui permet un changement rapide et minimise les temps d'arrêt.
Mesures de protection et normes de sécurité de la CEO
Les mesures de protection de la bande d'exposition professionnelle (OEB) sont essentielles pour protéger le personnel travaillant avec des ingrédients pharmaceutiques actifs à haute puissance (HPAPI) et des composés dangereux. Les solutions de confinement modernes sont conçues pour répondre aux exigences strictes de l'OEB, en fournissant une protection par couches grâce à des contrôles techniques, des processus validés et une surveillance continue.
Les éléments clés des mesures de protection de la CEO sont les suivants
Dispositifs de transfert en circuit fermé et des isolateurs de boîtes à gants afin d'éliminer le contact direct de l'opérateur avec les matières dangereuses.
Systèmes BIBO pour l'entretien des filtres, en veillant à ce que tous les fluides contaminés soient confinés en toute sécurité et éliminés sans risque d'exposition.
Environnements à pression négative et les sas d'entrée pour éviter la propagation des contaminants aéroportés.
Protocoles de nettoyage et de décontamination validés pour tous les équipements et surfaces en contact avec les composés puissants.
Surveillance en temps réel de l'environnement et de l'exposition afin de garantir que les concentrations dans l'air restent en deçà des seuils acceptables de la CEO.
La conformité aux normes de sécurité de la CEO est confirmée par des évaluations rigoureuses des risques, la qualification des performances et la validation continue. Les normes internationales telles que le Guide des bonnes pratiques de l'ISPE, la norme ICH Q9 sur la gestion des risques de qualité et la norme ISO 45001 sur les systèmes de gestion de la santé et de la sécurité au travail fournissent le cadre nécessaire à la conception et au maintien de stratégies de confinement conformes.
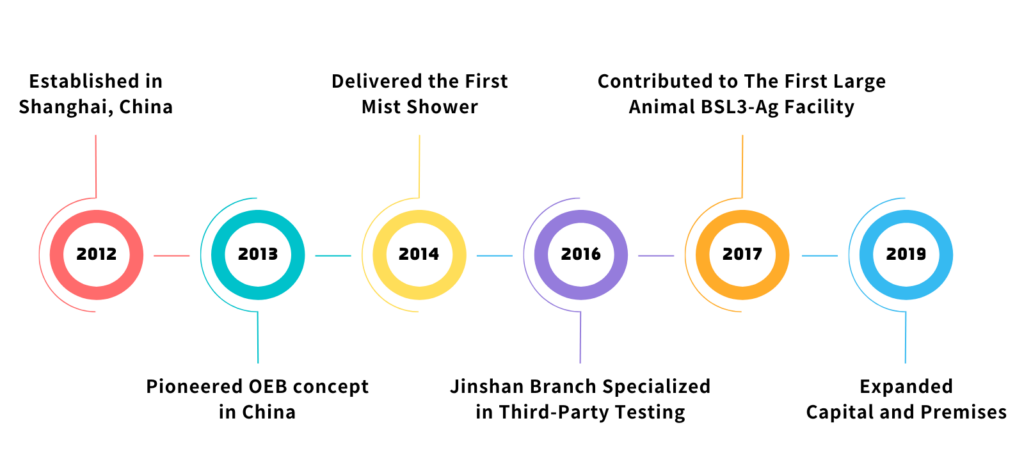
Historique
Explorez notre galerie des triomphes : Plongez dans notre sélection de projets récents, où notre approche ciblée et notre expertise ont permis à nos clients d'obtenir de bons résultats. Chaque cas témoigne de notre engagement à fournir des solutions solides et efficaces.

A propos de QUALIA
QUALIA est composée d'un ensemble de 42 experts dans les domaines de l'ingénierie pharmaceutique et de la biosécurité. Notre expertise approfondie englobe la conception, la construction, la gestion, ainsi que des services de conseil et de validation à l'échelle locale et mondiale. Nous sommes déterminés à fournir des solutions complètes adaptées à l'ingénierie des systèmes propres de biosécurité. Notre portefeuille comprend un assortiment varié de produits tels que des dispositifs de purification, des dispositifs de biosécurité, des systèmes CVC, des systèmes d'automatisation, des services de validation, des appareils de traitement et des tuyauteries stériles. Nous sommes fiers de notre capacité à concevoir des produits et des systèmes exclusifs qui répondent spécifiquement aux demandes nuancées de nos clients des secteurs pharmaceutique et de la biosécurité.
Questions fréquemment posées
Comment choisir le bon équipement de salle blanche pour la fabrication de produits pharmaceutiques ?
Lors de la sélection d'un équipement de salle blanche pour la fabrication de produits pharmaceutiques, il convient de tenir compte de trois facteurs essentiels : la classification de propreté requise (ISO 5-8), les besoins de confinement spécifiques au processus et les exigences de conformité réglementaire. Évaluez l'équipement en fonction de la compatibilité des matériaux avec les agents de nettoyage, de l'accessibilité de la maintenance et de la documentation de validation. Nos spécialistes biopharmaceutiques recommandent de procéder à une évaluation complète des risques afin d'identifier les sources potentielles de contamination avant de finaliser les spécifications de l'équipement.
Quelles sont les principales différences entre les systèmes BIBO et les filtres traditionnels ?
Les systèmes BIBO (Bag In Bag Out) offrent un confinement supérieur lors du remplacement des filtres par rapport aux boîtiers traditionnels en utilisant un système d'ensachage scellé qui empêche tout contact direct avec les filtres contaminés. Cela réduit considérablement l'exposition de l'opérateur aux matières dangereuses et préserve l'intégrité de la salle blanche pendant la maintenance. Les boîtiers de filtres traditionnels nécessitent un arrêt de l'environnement pendant les changements, alors que les systèmes BIBO permettent un fonctionnement continu, améliorant l'efficacité et réduisant les temps d'arrêt de la production.
À quelle fréquence les équipements de salle blanche doivent-ils être revalidés ?
Les équipements de salles blanches biopharmaceutiques doivent être soumis à une revalidation selon un calendrier basé sur les risques, généralement une fois par an pour les systèmes critiques et après toute modification importante. Les systèmes de surveillance continue peuvent fournir des données permettant d'optimiser la fréquence de revalidation en fonction des performances réelles plutôt que de délais arbitraires. Les exigences réglementaires peuvent spécifier des intervalles de revalidation minimaux en fonction de vos processus spécifiques et des profils de risque de vos produits.
Quel est le niveau de confinement approprié pour les composés OEB 4 ?
Les composés OEB 4 nécessitent des solutions de confinement complètes comprenant des systèmes fermés, des environnements à pression négative et des technologies de barrières redondantes. Le confinement approprié comprend des systèmes de filtration BIBO dédiés, des sas avec des mécanismes de verrouillage des portes et une surveillance continue des pressions différentielles. Le personnel travaillant avec des matériaux OEB 4 doit utiliser des EPI appropriés et suivre des procédures opérationnelles standard strictes pour la manipulation des matériaux et les protocoles de décontamination.
En quoi les exigences des laboratoires BSL-3 et BSL-4 diffèrent-elles en ce qui concerne le matériel de confinement ?
Les laboratoires BSL-4 nécessitent des mesures de confinement beaucoup plus strictes que les laboratoires BSL-3, notamment des enceintes de sécurité biologique de classe III ou des combinaisons à pression positive avec des sources d'air dédiées. Tous deux exigent une filtration HEPA pour l'air évacué, mais le BSL-4 requiert des systèmes de filtration redondants avec des exigences de validation supplémentaires. Les installations BSL-4 doivent mettre en œuvre des capacités de décontamination complètes, tandis que les installations BSL-3 peuvent utiliser des procédures de décontamination localisées basées sur l'évaluation des risques.