Високоефективне біофармацевтичне обладнання та системи для чистих приміщень
QUALIA постачає передове біофармацевтичне обладнання для чистих приміщень, розроблене відповідно до найсуворіших вимог безпеки та нормативних вимог у галузі. Наш комплексний асортимент рішень включає спеціалізовані системи ізоляції для лабораторій BSL-3 і BSL-4, що поєднують в собі передові технології з практичними конструкціями, які підвищують безпеку і ефективність роботи. Маючи багаторічний досвід у створенні інфраструктури чистих приміщень і захисних заходів для ОЕБ, ми надаємо фармацевтичним і біотехнологічним компаніям надійне обладнання, яке забезпечує повний захист протягом усіх критично важливих виробничих процесів.
Спільне проектування та
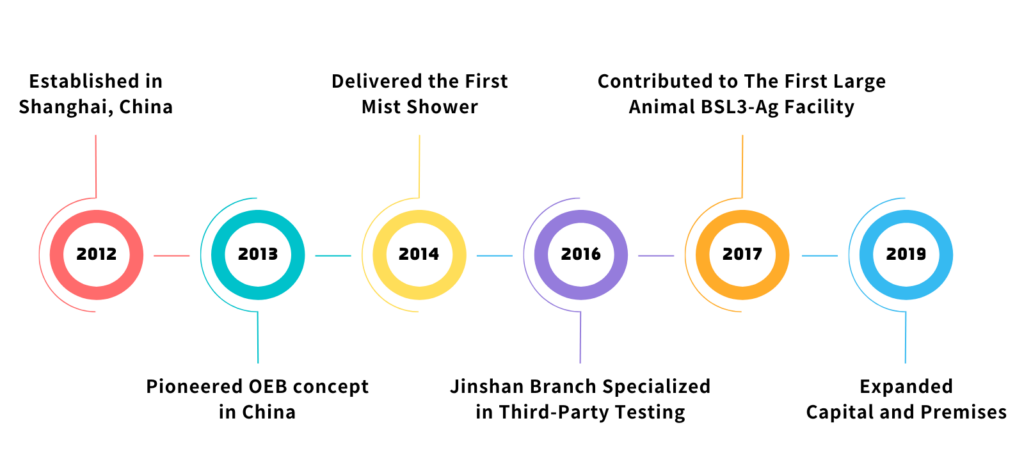
Будівництво першого в Китаї приміщення для великих тварин BSL3-Ag.
Надавав основні послуги 70+ світовим лабораторіям BSL3 та майстерням з виробництва вакцин.
Глобальна мережа з 210+ клієнтів, посилена стратегічними партнерськими відносинами.
Надано понад 1800 дверей APR, 930 туманних душових кабін, 850 BIBO та 400 VHP прохідних боксів.
Вимоги до валідації біофармацевтичних чистих приміщень
Впровадження належних вимог до валідації біофармацевтичних чистих приміщень має важливе значення для дотримання нормативних вимог і збереження цілісності продукції. Наші протоколи валідації гарантують, що ваше обладнання для чистих приміщень відповідає суворим галузевим стандартам, підтримуючи при цьому операційну ефективність.
Передові дослідження та розробки
Передові продукти, розроблені глобальною командою експертів.
Бренд, якому довіряють
Довгострокові відносини з лояльною клієнтською базою у фармацевтичному та медичному секторах.
Експертиза у сфері захисту
Великий досвід роботи з лабораторними стандартами P3, P4 та галузевими нормативами OEB.
Універсальне рішення
Комплексні проекти "під ключ" для чистих приміщень і супутнього обладнання.
Потужність QUALIA
Обладнання та рішення для чистих приміщень
Серія Air
Система фільтрації на місці
Серія ISO
cRABS
Ізолятор OEB4/5
Ізолятор біобезпеки
Серія "Замок
Біобезпечний ізоляційний демпфер
Механічне ущільнення дверей APR
Пневматичне ущільнення дверей APR
Модульна лабораторія
Мобільна модульна лабораторія
Серія Pass
Біозахисний відстійник для занурення
VHP Pass Box
Скринька для перепусток з біозахисту
Душова серія
Туманний душ
Хімічний душ
Водяний душ
Серія "Замок
Генератор VHP Тип I
Генератор VHP Тип II III
Очищення води
Трубопровідний фільтр HEPA на місці
Bag-In/Bag-Out - системи BIBO в середовищах BSL-3/BSL-4

Типова заміна фільтра BIBO передбачає герметичне приєднання зовнішнього мішка до корпусу, виймання використаного фільтра у внутрішній мішок, а потім надійне запечатування та виймання упакованого фільтра для безпечної утилізації. Цей процес підтримується портами для рукавичок і чіткими СОПами, що зводить до мінімуму людські помилки та ризик опромінення. Результатом є перевірена, повторювана процедура, яка відповідає або перевищує міжнародні стандарти біобезпеки та інженерні стандарти, такі як ISO 14644, ASME AG-1 та IEST-RP-CC001.
Комплексні рішення з локалізації для біофармацевтичного виробництва
Біофармацевтичне виробництво вимагає безкомпромісного контролю повітряних часток, перехресного забруднення та професійного впливу. Комплексні рішення з локалізації включають в себе кілька рівнів інженерного контролю, в тому числі системи BIBO, високоефективну фільтрацію повітря від твердих частинок (HEPA/ULPA), зони від'ємного тиску і спеціальні ізолятори. Ці системи призначені для захисту цілісності продукції та безпеки персоналу протягом усього технологічного ланцюжка - від обробки сировини до пакування готової продукції.
Ці рішення розроблені відповідно до світових стандартів, таких як EU GMP Annex 1, FDA 21 CFR Part 211 та ISO 14644. Результатом є виробниче середовище, яке підтримує регуляторні перевірки, знижує ризик втрати партії та підвищує загальну продуктивність.
IOS 14644
Стандарт чистого приміщення
Фільтрувальні установки BIBO для всіх критично важливих потоків витяжного та припливного повітря, забезпечуючи безпечне обслуговування фільтрів і підтверджену герметичність.
Індивідуальні ізолятори та бар'єрні системи для асептичної обробки, роботи з АФІ та управління сильнодіючими сполуками.
Керування каскадом тиску для підтримання спрямованого потоку повітря та запобігання перехресному забрудненню між чистими та брудними зонами.
Постійний екологічний моніторинг для виявлення в реальному часі кількості частинок, відхилень тиску та продуктивності системи.
Затверджені протоколи знезараження для поверхонь обладнання та об'єктів, забезпечуючи швидку переналадку та мінімізуючи час простою.
Захисні заходи та стандарти безпеки ОЕБ
Заходи захисту від професійного впливу (Occupational Exposure Band, OEB) необхідні для захисту персоналу, який працює з сильнодіючими активними фармацевтичними інгредієнтами (HPAPI) та небезпечними сполуками. Сучасні засоби захисту розроблені відповідно до суворих вимог OEB, забезпечуючи багаторівневий захист завдяки інженерному контролю, валідованим процесам і безперервному моніторингу.
Ключові елементи захисних заходів ОЕБ включають
Пристрої передачі в замкненій системі та ізолятори для рукавичок, щоб уникнути прямого контакту оператора з небезпечними матеріалами.
Системи BIBO для обслуговування фільтрів, гарантуючи, що всі забруднені носії надійно утримуються та утилізуються без ризику контакту з ними.
Середовища з від'ємним тиском і шлюзові системи входу, щоб запобігти поширенню забруднюючих речовин повітряним шляхом.
Затверджені протоколи очищення та знезараження для всього обладнання та поверхонь, що контактують з сильнодіючими сполуками.
Моніторинг навколишнього середовища та впливу в реальному часі для забезпечення того, щоб концентрації в повітрі залишалися в межах допустимих порогових значень ОЕБ.
Відповідність стандартам безпеки OEB підтверджується ретельною оцінкою ризиків, кваліфікацією персоналу та постійною перевіркою. Міжнародні стандарти, такі як ISPE Good Practice Guide, ICH Q9 Quality Risk Management та ISO 45001 Occupational Health and Safety Management Systems, забезпечують основу для розробки та підтримки відповідних стратегій локалізації.
Послужний список
Перегляньте нашу Галерею тріумфів: Пориньте в нашу добірку нещодавніх успішних проектів, де наш цілеспрямований підхід та досвід привели до успішних результатів для наших клієнтів. Кожен випадок є свідченням нашого прагнення надавати надійні та ефективні рішення.

Про QUALIA
QUALIA складається з 42 експертів у галузі фармацевтичної інженерії та біозахисту. Наш глибокий досвід охоплює проектування, будівництво, управління, а також послуги з консалтингу та валідації на місцевому та глобальному рівнях. Ми наполегливо надаємо комплексні рішення, розроблені з урахуванням вимог біозахисту та чистого системного інжинірингу. Наше портфоліо включає різноманітний асортимент продукції, такої як пристрої для очищення, засоби біозахисту, системи опалення, вентиляції та кондиціонування повітря, системи автоматизації, послуги з валідації, технологічне обладнання та стерильні трубопроводи. Ми пишаємося нашою здатністю розробляти запатентовані продукти і системи, які спеціально задовольняють тонкі вимоги наших клієнтів у фармацевтичній та біозахисній галузях.
Поширені запитання
Як правильно вибрати обладнання для чистих приміщень для фармацевтичного виробництва?
Обираючи обладнання для чистих приміщень для фармацевтичного виробництва, враховуйте три важливі фактори: необхідну класифікацію чистоти (ISO 5-8), потреби в ізоляції для конкретного процесу та вимоги щодо відповідності нормативним вимогам. Оцінюйте обладнання на основі сумісності матеріалів з миючими засобами, доступності технічного обслуговування та наявності валідаційної документації. Наші фахівці з біофармацевтики рекомендують проводити комплексну оцінку ризиків для виявлення потенційних джерел забруднення перед тим, як завершити розробку специфікацій обладнання.
Які ключові відмінності між системами BIBO та традиційними корпусами фільтрів?
Системи BIBO (Bag In Bag Out) забезпечують кращу ізоляцію під час заміни фільтрів порівняно з традиційними корпусами завдяки використанню герметичної системи мішків, яка запобігає прямому контакту із забрудненими фільтрами. Це значно зменшує вплив небезпечних матеріалів на оператора і підтримує цілісність чистого приміщення під час технічного обслуговування. Традиційні корпуси фільтрів вимагають екологічного відключення під час заміни, тоді як системи BIBO дозволяють безперервну роботу, підвищуючи ефективність і скорочуючи час простою виробництва.
Як часто слід проводити повторну перевірку обладнання для чистих приміщень?
Біофармацевтичне обладнання для чистих приміщень повинно проходити повторну перевірку згідно з графіком, заснованим на оцінці ризиків, як правило, щорічно для критично важливих систем і після будь-яких значних модифікацій. Системи безперервного моніторингу можуть надавати інформацію на основі даних для оптимізації частоти повторних перевірок на основі фактичних показників, а не довільних графіків. Регуляторні вимоги можуть визначати мінімальні інтервали повторної перевірки залежно від ваших конкретних процесів і профілів ризику продукції.
Який рівень ізоляції підходить для сполук OEB 4?
З'єднання OEB 4 вимагають комплексних рішень з утримання, включаючи закриті системи, середовища з від'ємним тиском і технології резервних бар'єрів. Відповідна ізоляція включає спеціальні системи фільтрації BIBO, шлюзи з блокуванням дверних механізмів і безперервний моніторинг перепаду тиску. Персонал, який працює з матеріалами OEB 4, повинен використовувати належні засоби індивідуального захисту і дотримуватися суворих стандартних операційних процедур поводження з матеріалами та протоколів дезактивації.
Чим відрізняються лабораторні вимоги BSL-3 і BSL-4 до обладнання для локалізації?
Лабораторії BSL-4 вимагають значно суворіших заходів ізоляції, ніж BSL-3, включаючи шафи біологічної безпеки класу III або костюми надлишкового тиску зі спеціальною подачею повітря. В обох випадках для відпрацьованого повітря потрібна фільтрація HEPA, але BSL-4 вимагає резервних систем фільтрації з додатковими вимогами до валідації. На об'єктах BSL-4 повинні бути реалізовані можливості повної дезактивації об'єкта, в той час як на об'єктах BSL-3 можуть використовуватися локальні процедури дезактивації на основі оцінки ризиків.