Leistungsstarke biopharmazeutische Reinraumgeräte und -systeme
QUALIA liefert fortschrittliche biopharmazeutische Reinraumanlagen, die den strengsten Sicherheits- und Regulierungsanforderungen der Branche entsprechen. Unser umfassendes Angebot an Lösungen umfasst spezialisierte Containment-Systeme für BSL-3- und BSL-4-Labore, die modernste Technologie mit praktischen Designs verbinden, die sowohl die Sicherheit als auch die betriebliche Effizienz verbessern. Dank unserer jahrzehntelangen Erfahrung mit Reinrauminfrastrukturen und OEB-Schutzmaßnahmen können wir Pharma- und Biotechnologieunternehmen zuverlässige Anlagen zur Verfügung stellen, die den vollständigen Schutz kritischer Herstellungsprozesse gewährleisten.
Kollaboratives Design und
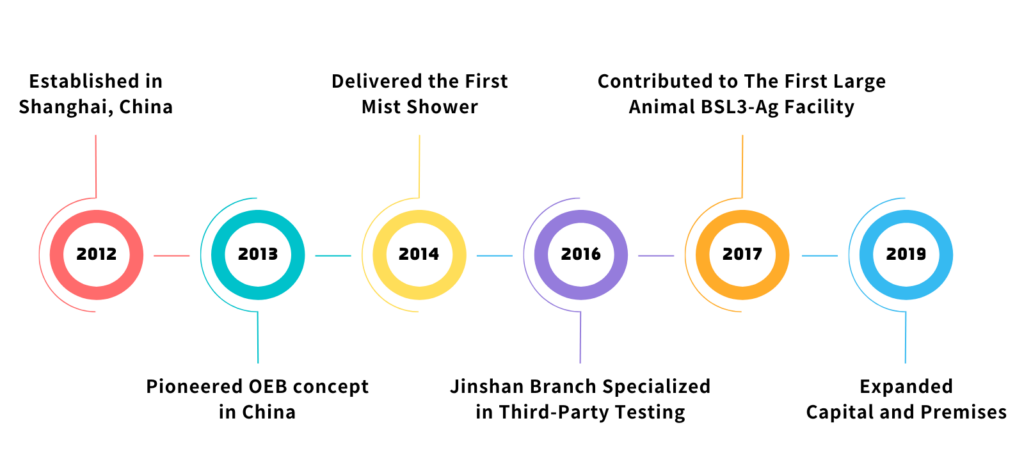
Bau von Chinas erstem BSL3-Ag-Großtierraum.
Kerndienstleistungen für mehr als 70 globale BSL3-Labors und Impfstoffproduktionswerkstätten.
Ein globales Netzwerk von über 210 Kunden, das durch strategische Partnerschaften gestärkt wird.
Bereitstellung von über 1800 APR-Türen, 930 Nebelduschen, 850 BIBO und 400 VHP-Passboxen.
Anforderungen an die Validierung von biopharmazeutischen Reinräumen
Die Umsetzung ordnungsgemäßer Anforderungen an die Validierung von Reinräumen in der Biopharmazie ist für die Einhaltung gesetzlicher Vorschriften und die Produktintegrität unerlässlich. Unsere Validierungsprotokolle stellen sicher, dass Ihre Reinraumausrüstung die strengen Industriestandards erfüllt und gleichzeitig die betriebliche Effizienz unterstützt.
Fortgeschrittene F&E
Führende Produkte, entwickelt von einem globalen Expertenteam.
Vertrauenswürdige Marke
Langjährige Beziehungen zu einem treuen Kundenstamm in der Pharma- und Gesundheitsbranche.
Fachwissen im Bereich Schutz
Umfassende Erfahrung mit P3- und P4-Labornormen und OEB-Branchenvorschriften.
Lösung aus einer Hand
Komplette schlüsselfertige Projekte für Reinräume und zugehörige Ausrüstung.
Kapazität von QUALIA
Reinraum Ausrüstungen & Lösungen
Serie Air
In-Situ-Filtrationssystem
ISO-Reihe
cRABS
OEB4/5 Isolator
Biosicherheits-Isolator
Schloss-Serie
Biosicherheits-Isolationsdämpfer
Gleitringdichtung APR-Türen
Pneumatische Dichtung APR-Türen
Modul Labor
Mobiles Modul-Labor
Pass-Serie
Biosicherheitstank
VHP-Pass-Box
Biosicherheits-Pass-Box
Dusche Serie
Nebel-Dusche
Chemische Dusche
Wasserdusche
Schloss-Serie
VHP-Generator Typ I
VHP-Generator Typ II III
Wasseraufbereitung
In-Situ-Rohrleitung HEPA
Bag-In/Bag-Out - BIBO-Systeme in BSL-3/BSL-4-Umgebungen

Ein typischer BIBO-Filterwechsel umfasst das Versiegeln des Außenbeutels mit dem Gehäuse, die Entnahme des verbrauchten Filters in den Innenbeutel und dann das sichere Versiegeln und Entfernen des Beutelfilters zur sicheren Entsorgung. Dieser Prozess wird durch Handschuhanschlüsse und klare SOPs unterstützt, wodurch menschliche Fehler und Expositionsrisiken minimiert werden. Das Ergebnis ist ein validiertes, wiederholbares Verfahren, das die internationalen Normen für biologische Sicherheit und Technik wie ISO 14644, ASME AG-1 und IEST-RP-CC001 erfüllt oder übertrifft.
Umfassende Containment-Lösungen für die biopharmazeutische Produktion
Die biopharmazeutische Produktion erfordert eine kompromisslose Kontrolle von luftgetragenen Partikeln, Kreuzkontaminationen und beruflicher Belastung. Umfassende Containment-Lösungen integrieren mehrere Ebenen von technischen Kontrollen, einschließlich BIBO-Systemen, hocheffizienter Partikelfilterung (HEPA/ULPA), Unterdruckzonen und kundenspezifischen Isolatoren. Diese Systeme sind so konzipiert, dass sie sowohl die Produktintegrität als auch die Sicherheit des Personals über die gesamte Prozesskette hinweg schützen - von der Handhabung des Rohmaterials bis zur Verpackung des Endprodukts.
Diese Lösungen sind so konzipiert, dass sie den globalen Standards wie EU GMP Annex 1, FDA 21 CFR Part 211 und ISO 14644 entsprechen. Das Ergebnis ist eine Produktionsumgebung, die behördliche Inspektionen unterstützt, das Risiko von Chargenverlusten reduziert und die Gesamtproduktivität steigert.
IOS 14644
Reinraum-Standard
BIBO-Filteranlagen für alle kritischen Ab- und Zuluftströme, die eine sichere Filterwartung und validierte Eindämmung gewährleisten.
Kundenspezifische Isolatoren und Barrieresysteme für die aseptische Verarbeitung, die Handhabung von Wirkstoffen und die Verwaltung potenter Substanzen.
Druckkaskadenmanagement um einen gerichteten Luftstrom aufrechtzuerhalten und eine Kreuzkontamination zwischen sauberen und schmutzigen Bereichen zu verhindern.
Kontinuierliche Umweltüberwachung zur Echtzeit-Erkennung von Partikelzahlen, Druckabweichungen und Systemleistung.
Validierte Dekontaminationsprotokolle für Geräte- und Anlagenoberflächen, die eine schnelle Umrüstung ermöglichen und die Ausfallzeiten minimieren.
OEB-Schutzmaßnahmen und Sicherheitsstandards
OEB-Schutzmaßnahmen (Occupational Exposure Band) sind für den Schutz des Personals, das mit hochwirksamen pharmazeutischen Wirkstoffen (HPAPIs) und gefährlichen Verbindungen arbeitet, unerlässlich. Moderne Containment-Lösungen sind so konzipiert, dass sie die strengen OEB-Anforderungen erfüllen und durch technische Kontrollen, validierte Prozesse und kontinuierliche Überwachung einen mehrschichtigen Schutz bieten.
Zu den wichtigsten Elementen der OEB-Schutzmaßnahmen gehören:
Geschlossene Transfersysteme und Handschuhkastenisolatoren, um den direkten Kontakt des Bedieners mit Gefahrstoffen zu verhindern.
BIBO-Systeme für die Filterwartung, um sicherzustellen, dass alle kontaminierten Medien sicher eingeschlossen und ohne Expositionsrisiko entsorgt werden.
Umgebungen mit Unterdruck und Schleusensysteme, um die Ausbreitung von Luftschadstoffen zu verhindern.
Validierte Reinigungs- und Dekontaminationsprotokolle für alle Geräte und Oberflächen, die mit starken Verbindungen in Berührung kommen.
Umwelt- und Expositionsüberwachung in Echtzeit um sicherzustellen, dass die Konzentrationen in der Luft innerhalb der zulässigen OEB-Grenzwerte bleiben.
Die Einhaltung der OEB-Sicherheitsstandards wird durch strenge Risikobewertungen, Leistungsqualifizierung und laufende Validierung bestätigt. Internationale Normen wie der ISPE Good Practice Guide, ICH Q9 Quality Risk Management und ISO 45001 Occupational Health and Safety Management Systems bilden den Rahmen für die Entwicklung und Aufrechterhaltung konformer Einschließungsstrategien.
Erfolgsbilanz
Entdecken Sie unsere Galerie der Triumphe: Tauchen Sie ein in eine Auswahl unserer jüngsten Erfolgsprojekte, bei denen unser fokussierter Ansatz und unsere Expertise zu erfolgreichen Ergebnissen für unsere Kunden geführt haben. Jeder Fall ist ein Beweis für unser Engagement, solide und effektive Lösungen anzubieten.

Über QUALIA
QUALIA besteht aus einem engagierten Team von 42 Experten auf dem Gebiet der Pharma- und Biosicherheitstechnik. Unser fundiertes Fachwissen umfasst Planung, Bau und Management sowie lokale und globale Beratungs- und Validierungsdienste. Wir sind bestrebt, umfassende, auf die Biosicherheit zugeschnittene Lösungen für die Reinraumtechnik zu liefern. Unser Portfolio umfasst ein vielfältiges Sortiment an Produkten wie Reinigungsgeräte, Biosicherheitsvorrichtungen, HVAC-Systeme, Automatisierungssysteme, Validierungsdienste, Prozessapparate und sterile Rohrleitungen. Wir sind stolz auf unsere Fähigkeit, firmeneigene Produkte und Systeme zu entwickeln, die speziell auf die differenzierten Anforderungen unserer Kunden in der Pharma- und Biosicherheitsbranche abgestimmt sind.
Häufig gestellte Fragen
Wie wählt man die richtige Reinraumausrüstung für die pharmazeutische Produktion aus?
Bei der Auswahl von Reinraumausrüstungen für die pharmazeutische Produktion sind drei entscheidende Faktoren zu berücksichtigen: die erforderliche Reinheitsklassifizierung (ISO 5-8), prozessspezifische Containment-Anforderungen und die Einhaltung gesetzlicher Vorschriften. Bewerten Sie die Ausrüstung auf der Grundlage der Materialverträglichkeit mit Reinigungsmitteln, der Wartungszugänglichkeit und der Validierungsdokumentation. Unsere Biopharmazie-Spezialisten empfehlen, eine umfassende Risikobewertung durchzuführen, um potenzielle Kontaminationsquellen zu identifizieren, bevor die Spezifikationen für die Ausrüstung festgelegt werden.
Was sind die wichtigsten Unterschiede zwischen BIBO-Systemen und herkömmlichen Filtergehäusen?
BIBO-Systeme (Bag In Bag Out) bieten im Vergleich zu herkömmlichen Gehäusen einen besseren Schutz beim Filterwechsel, da ein versiegeltes Beutelsystem verwendet wird, das den direkten Kontakt mit kontaminierten Filtern verhindert. Dadurch wird die Exposition des Bedieners gegenüber gefährlichen Stoffen erheblich reduziert und die Integrität des Reinraums während der Wartung aufrechterhalten. Bei herkömmlichen Filtergehäusen muss die Umgebung während des Wechsels abgeschaltet werden, während BIBO-Systeme einen kontinuierlichen Betrieb ermöglichen, was die Effizienz steigert und Produktionsausfallzeiten reduziert.
Wie oft sollte die Reinraumausrüstung revalidiert werden?
Biopharmazeutische Reinraumausrüstungen sollten nach einem risikobasierten Zeitplan revalidiert werden, in der Regel jährlich für kritische Systeme und nach allen wesentlichen Änderungen. Kontinuierliche Überwachungssysteme können datengestützte Erkenntnisse zur Optimierung der Revalidierungshäufigkeit auf der Grundlage der tatsächlichen Leistung statt willkürlicher Zeitvorgaben liefern. Gesetzliche Vorschriften können Mindestintervalle für die Revalidierung vorschreiben, die von Ihren spezifischen Prozessen und Produktrisikoprofilen abhängen.
Welche Einschließungsstufe ist für OEB 4-Verbindungen angemessen?
OEB 4-Verbindungen erfordern umfassende Containment-Lösungen, einschließlich geschlossener Systeme, Unterdruckumgebungen und redundanter Barrieretechniken. Geeignete Containment-Lösungen umfassen spezielle BIBO-Filtersysteme, Schleusen mit verriegelten Türmechanismen und eine kontinuierliche Überwachung von Differenzdrücken. Das Personal, das mit OEB 4-Materialien arbeitet, sollte angemessene PSA verwenden und strenge Standardarbeitsanweisungen für die Materialhandhabung und Dekontaminationsprotokolle befolgen.
Wie unterscheiden sich die Anforderungen von BSL-3- und BSL-4-Labors an die Containment-Ausrüstung?
BSL-4-Laboratorien erfordern wesentlich strengere Einschließungsmaßnahmen als BSL-3-Laboratorien, einschließlich biologischer Sicherheitswerkbänke der Klasse III oder Überdruckanzüge mit spezieller Luftversorgung. Beide erfordern HEPA-Filterung für die Abluft, aber BSL-4 erfordert redundante Filtersysteme mit zusätzlichen Validierungsanforderungen. BSL-4-Einrichtungen müssen eine vollständige Dekontaminierung der Einrichtung durchführen, während BSL-3-Einrichtungen je nach Risikobewertung lokalisierte Dekontaminationsverfahren anwenden können.